はじめに
みなさんは高分子というものはご存知でしょうか?
高分子はペットボトルや衣服など幅広く用いられている物質であり、私たちの生活とは切り離せないものになっています。
しかし、高分子は非常に複雑なものであるため、その詳細を把握している方は中々いないでしょう。
そこで今回は、高分子がどういうものなのか解説していきたいと思います。
高分子とは?
高分子の定義は国際純正・応用化学連合(IUPAC)を参考にしますと、「分子量が大きい分子で、分子量が小さい分子から実質的または概念的に得られる単位の多数回の繰り返しで構成した構造」になります。
…非常にわかりにくいですね。
ではこの高分子の定義を噛み砕いて説明していきます。
まず高分子を解釈する上で必要な各単語の説明からです。
分子
分子は物質の最小構成単位である原子2つ以上から構成される物質です。
例えば、私たちが日常的に使用している水はH2Oという分子式で示され、水素原子(H)2個と酸素原子(O)で構成されています。
しかし、原子が2つ以上付いていれば何でも分子になるわけではありません。
通常、共有結合によって結合した原子は分子として定義されますが、水素結合やイオン結合などの非共有結合のものは分子とは言いません。
分子に見えるけれども分子ではない物質の例には、塩化ナトリウム(NaCl)があります。
一見するとナトリウム原子と塩素原子が共有結合した分子に見えますが、イオン結合で結合しています。
イオン結合で結合したものは、分子とは異なり、それが1つの塊になりません。
水であれば、H2Oという分子が1つ1つ塊として存在していますが、塩化ナトリウムは-Na-Cl-Na-Cl-というように結合しており、塊状にはなっていません。
そのため、塩化ナトリウムは塩素原子とナトリウム原子の数によって際限なく大きくなり、様々な形をとります。
このような理由によって、共有結合で結合していない原子は分子とは呼びません。
分子量
分子量は分子中の原子量の総和のことを言います。
では原子量とは何なのかですが、「一定の基準によって定めた原子の質量」を指します。
この一定の基準とは、炭素の相対質量のことです。
“相対質量”って何?となりそうですが、ここでは一旦置いておきます。
炭素の相対質量を12と定義した際の原子の質量を計算したものが原子量となります。
例えば、水素の原子量1というのも、炭素の相対質量12から計算して求められた値になります。
そして、分子量は原子量の和になりますので、例えば水ですと分子量は、水素原子(原子量1)2個、酸素原子(原子量16)1個の合計である18となります。
モノマー(単量体)
高分子は英語でポリマー(polymer)と言い、その最小構成単位をモノマー(monomer)と言います。
分子とモノマーは何が違うのかですが、分子という大きな括りの中に、モノマーという高分子を形成する物が含まれていると考えてください。
モノマーの特徴ですが、分子量を大きくするために、モノマー同士が反応できる部位を有しています。
例として、モノマーの中でも特に単純な構造をもつエチレンを以下に示します。
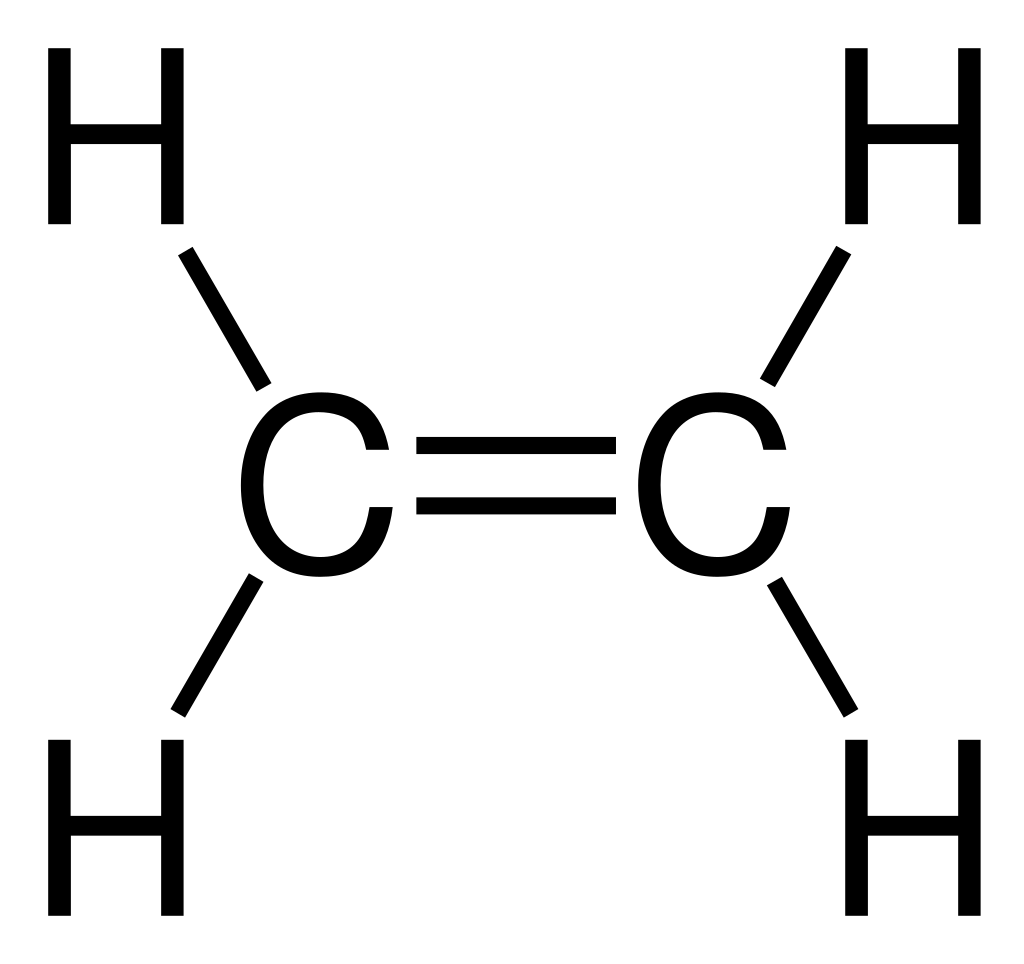
上の画像を見ると、エチレンの炭素原子が2本の結合で繋がれています。
この二重結合の部位をビニル基と言い、高分子を形成する基になります。
このビニル基から電子が移動することで高分子を形成することが可能になるのです。
高分子
高分子は上で示したモノマーが多数連なり、分子量が非常に大きくなったものを言います。
「大きいとはどの程度?」と思うかもしれませんが、具体的な分子量は定義されていません。
しかし、一般的には分子量1万を超えてくると高分子として定義されるようになります。
また分子量が1万に届かない数千程度のものをオリゴマーと言います。
そして高分子は、”重合”というモノマー同士の反応によって作られます。
重合
モノマー同士が結合してより分子量が大きい分子を作る反応を重合と言います。
この重合反応ですが、反応の仕方によって連鎖重合と逐次重合とに分けられます。
各重合の特徴を以下にまとめます。
- 連鎖重合:モノマーの二重結合から移動した電子(ラジカル)によって連鎖的にモノマーが反応し、分子量が大きくなる反応
- 逐次重合:ビニル基とは異なる反応部位を持った2種類以上のモノマーが相互に結合することで分子量が大きくなる反応
更に、連鎖重合にはラジカル重合、アニオン重合、カチオン重合などに分かれ、逐次重合は重縮合、重付加、付加縮合などに分かれます。
これらの反応については、また別の記事で紹介いたします。
まとめ
今回は私たち身の回りにある高分子の導入部分の説明をいたしました。これからも重合について解説していきますので、ぜひ参考にしてください。


